Tomando en consideración que según Brandwein (1988),
existen más de 50,000 compuestos químicos inorgánicos en los que no interviene
el carbono, se ha buscado un sistema para agruparlos de acuerdo con sus
propiedades químicas, para darles nombre y reconocerlos.
Se ha dado el nombre de función inorgánica al grupo de compuestos similares que presentan un conjunto de propiedades comunes. Las principales funciones químicas inorgánicas son: función óxido, función anhídrido, función hidróxido, función ácido y función sal.
Se ha dado el nombre de función inorgánica al grupo de compuestos similares que presentan un conjunto de propiedades comunes. Las principales funciones químicas inorgánicas son: función óxido, función anhídrido, función hidróxido, función ácido y función sal.
* Óxido:
E + O
* Óxido Base:
M + O = Óxido Base.
* Óxido Acido:
m + O = Óxido Ácido.
* Hidróxidos:
Óxido Base + H2O = Hidróxido.
* Ácidos:
Óxido. Ácido = Óxido. Ácido + H2O = Ácido. Ox. Ácido.
* Hidráxido:
H + VI A / VII A = Ácido Hidráxido.
*Sales Oxisales:
Ác. Óxac + Base = Óxido y Hidróxido = Sal Oxisal +
H2O.
* Sal Haloidea:
Ac. Hidróxido + Base = Óxido y Hidróxido = Sal
Haloidea + H2O.
*Cuando se hace reaccionar un metal con el oxígeno, se obtiene un óxido:
metal + oxígeno ———› óxido metálico
Na + ———›
sodio + oxígeno ———› óxido de sodio
**Nomenclatura:
Para formar el nombre del óxido se escribe la palabra "óxido" seguido de la preposición "de" y después el nombre del metal. Si el metal presenta más de dos valencias, se escribe entre paréntesis con número romano la valencia del metal con la que esté actuando
*Ejemplo:
-Función anhídrido:
Cuando se combinan un no metal con el oxiíeno se obtiene un anhídrido:
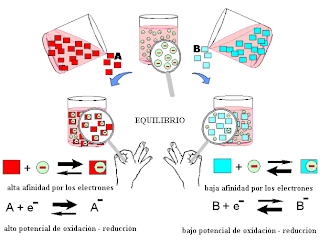
La oxidación es una reacción química donde un
compuesto cede electrones, y por lo tanto aumenta su estado de oxidación. La
reacción química opuesta a la oxidación se conoce como reducción, es decir
cuando una especie química acepta electrones. Estas dos reacciones siempre se
dan juntas, es decir, cuando una sustancia se oxida, siempre es por la acción
de otra que se reduce. Una cede electrones y la otra los acepta. Por esta
razón, se prefiere el término general de reacciones redox. La propia vida es un
fenómeno redox. El oxígeno es el mejor oxidante que existe debido a que la
molécula es poco reactiva (por su doble enlace) y sin embargo es muy
electronegativo, casi como el flúor.
La sustancia más oxidante que existe es el catión KrF+ porque fácilmente forma Kr y F+. Entre varias(KMnO4), el (Cr2O7), el agua oxigenada (H2O2), el ácido nítrico (HNO3), los hipohalitos y los halatos (por ejemplo el hipoclorito sódico (NaClO) muy oxidante en medio alcalino y el bromato potásico (KBrO3)). El ozono (O3) es un oxidante muy enérgico:
La sustancia más oxidante que existe es el catión KrF+ porque fácilmente forma Kr y F+. Entre varias(KMnO4), el (Cr2O7), el agua oxigenada (H2O2), el ácido nítrico (HNO3), los hipohalitos y los halatos (por ejemplo el hipoclorito sódico (NaClO) muy oxidante en medio alcalino y el bromato potásico (KBrO3)). El ozono (O3) es un oxidante muy enérgico:

No hay comentarios:
Publicar un comentario